Appunti sulla struttura dell'atomo
Gli studi sulla struttura dell'atomo hanno portato alla definizione di vari modelli, gli ultimi prevedono la presenza delle seguenti particelle:
Protoni: particelle con carica positiva
Neutroni: particelle con carica neutra
Elettroni: particelle con carica negativa
Tutti i modelli concordano sulla presenza di un nucleo composto da protoni e neutroni.
La massa di un elettrone è notevolmente inferiore a quella di un protone o neutrone, nella tabella seguente si vedono le cariche e la massa delle tre particelle:
| Particella | Simbolo | Carica | Massa |
| Elettrone | e- | − 1,6 x 10-19 C | 9,109 382 6 × 10−31 kg |
| Protone | p | 1,6 × 10−19 C | 1,672 623 1 × 10−27 kg |
| Neutrone | n | 0 C | 1,674 927 29 × 10−27 kg |
Gli elettroni sono disposti intorno al nucleo, i modelli divergono sul tipo di "traiettoria" che percorrono intorno al nucleo:
il modello di Bohr (1913):
prevede orbite circolari degli elettroni intorno al nucleo, ma non possono essere in qualsiasi posizione dello spazio, le orbite sono quantizzate, i raggi delle orbite sono proporzionali a numeri interi: 1, 2, 3, 4, 5, 6, 7. Questi valori vengono anche indicati come livelli energetici.
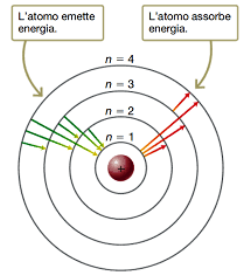
Un elettrone per passare da un’orbitale ad un' altro assorbe o cede energia:
- quando un elettrone assorbe un fotone, l’energia equivalente alla differenza delle 2 orbite, salta all’orbita superiore
- quando un elettrone cede un fotone, l’energia equivalente alla differenza delle 2 orbite, salta all’orbita inferiore
Le dimensioni di un atomo idealizzato con una sfera vengono riassunte nella seguente tabella:
| Particella | Diametro |
| Atomo | 10-10 m |
| Nucleo | 10-14 m |
| Protone | 10-15 m |
Il nucleo di un atomo è circa 10.000 volte più piccolo delle dimensioni di un atomo, poiché il volume è proporzionale al cubo dei diametri, la proporzione tra la materia solida e lo spazio vuoto in un atomo è pari a 10-12: un milionesimo di milionesimo.Questo significa che se dividiamo lo spazio occupato da un atomo in un milione di cellette e poi ogni celletta in un milione di parti, solo una di queste è occupata da materia, tutte le altre sono vuote!
Il modello Wilson-Sommerfeld (1915):
prevede orbitali elittici degli elettroni intorno al nucleo, secondo la meccanica quantistica non ha più senso di parlare di una traiettoria di una particella, non si è in grado di determinare contemporaneamente posizione e quantità di moto di una particella (principio di indeterminazione di Heisenberg). Gli orbitali sono regioni dello spazio in cui si ha la massima probabilità di trovare un elettrone in un certo punto dello spazio in un dato istante di tempo.
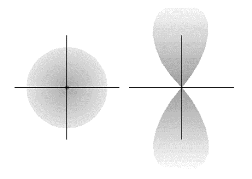
Un orbitale atomico viene approssimato con quella regione di spazio attorno al nucleo atomico in cui la probabilità di trovare un elettrone è massima (massima densità di probabilità) ed è delimitata da una superficie sulla quale il modulo dell'ampiezza della funzione d'onda (equazione di Schrödinger) è costante (generalmente normalizzata a uno). In altre parole, una regione di spazio attorno ad un nucleo atomico in cui la probabilità di trovarvi un elettrone è massima (di solito superiore ad un limite convenzionalmente fissato nel 95%) è usata per rappresentare graficamente un orbitale atomico di quell'elettrone.
La meccanica quantistica moderna si basa su modelli con orbitali elittici.
Numeri quantici
Gli orbitali sono modelli utili per cercare di localizzare gli elettroni anche se le nuvole elettroniche non hanno confini ben definiti dal momento che la probabilità di trovare gli elettroni anche al di fuori è bassa ma non nulla.
Ogni orbitale può essere definito (dimensione, forma e orientamento nello spazio) grazie a tre numeri quantici, che sono dei valori che, inseriti nell’equazione di Schroedinger ne permettono la risoluzione (esiste un quarto numero quantico utilizzato per gli elettroni).
Numero quantico principale: n
Esprime l'energia quantizzata di ogni livello energetico: all’aumentare di n, gli orbitali diventano più grandi, la loro energia aumenta e gli elettroni che in esso sono contenuti si allontanano dal nucleo. Tutti gli orbitali che sono caratterizzati dallo stesso valore di n appartengono allo stesso livello energetico ma, non necessariamente, hanno la stessa energia.
Può assumere valori che vanno da 1 a 7
Numero quantico secondario: l
Determina le caratteristiche geometriche (forma) dell’orbitale e definisce quanti orbitali di forma diversa (sottolivelli) possono esistere nello stesso livello energetico. La forma e il volume dei diversi tipi di orbitali sono molto differenti, i valori che può assumere sono interi (quantizzati) compresi tra 0 e n -1.
In un atomo non eccitato esistono 4 tipi di orbitali: l = 0 chiamato s (sharp), l = 1 chiamato p (principal), l = 3 chiamato d (diffuse), l = 4 chiamato f (fundamental)
-
-
- Gli orbitali s sono sferici con al centro della sfera il nucleo dell'atomo
- Gli orbitali p sono costituiti da un doppio lobo con il nucleo dell'atomo posizionato nel punto di contatto tra i 2 lobi
- Gli orbitali d hanno una forma a 4 lobi con il nucleo dell'atomo posizionato nel punto di contatto tra i 4 lobi
- Gli orbitali f hanno una forma complessa con più di 4 lobi
-
Numero quantico magnetico: ml
Un elettrone, avendo una carica elettrica, girando su un orbitale genera un campo magnetico quantizzato.
Può assumere valori compresi tra -l e +l e determinano il tipo di nodo, planare o conico, la sua orientazione nello spazio e la molteplicità degli orbitali; in particolare indica la direzione che l'orbitale può assumere nello spazio. Ad esempio:
per l=0 ml=0
esiste un solo orbitale "s" per ogni livello (per l=0 può assumere solo il valore 0) e infatti l'orbitale "s" è di forma sferica e quindi ha un'unica orientazione nello spazio.
per l=1 ml=-1 ,0, +1
esistono tre orbitali “p” per ogni livello con i doppi lobi orientati lungo i tre assi coordinati x, y, z (per l = 1, m può assumere i valori – 1, 0, + 1).
per l=2 ml=-2, -1, 0, +1, +2
esistono cinque orbitali “d” anche loro con diverso orientamento.
per l=3 ml=-3, -2, -1, 0, +1, +2, +3
esistono 7 orbitali f
Numero quantico di spin: ms
L’elettrone girando su se stesso in senso orario o antiorario genera un campo magnetico chiamato spin.
Può assumere solo due valori:
-
-
- + ½ rotazione in senso orario, indicata con una freccia rivolta verso l’alto
- – ½ rotazione in senso antiorario, indicata con una freccia rivolta verso il basso
-
Rappresentazione grafica degli orbitali in base ai numeri atomici:

Configurazioni elettroniche secondo il modello ad orbitali
Dato un atomo con i suoi livelli energetici, orbitali ed elettroni, in che orbitali si posizionano gli elettroni? Per rispondere a questa domanda bisogna prendere in considerazione i seguenti tre principi:
- Principio di Aufban (in tedesco "costruzione): gli orbitali vengono riempiti partendo da quelli ad energia minima (stato fondamentale) e riempiendo, via via, quelli ad energia superiore.
- Principio di Pauli: in ogni orbitale ci possono essere al massimo 2 elettroni, con spin opposto (in un atomo infatti non possono esistere due elettroni che presentano gli stessi quattro numeri quantici).
Il principio si applica solo ai fermioni( protoni, neutroni, elettroni), che formano stati quantici antisimmetrici e hanno spin semi-intero. - Principo di Hund: se sono presenti degli orbitali "degeneri" (ovvero più autostati per un unico autovalore, come ad esempio i tre orbitali p) gli elettroni si distribuiscono in modo tale da occupare il numero massimo di orbitali. In altre parole se ci sono più orbitali con la stessa energia (ad esempio, gli orbitali p), si colloca un elettrone su ciascun orbitale vuoto con lo stesso spin e solo in seguito si completano gli orbitali semipieni. Il principio di Hund della massima molteplicità afferma che, per minimizzare la repulsione, l’elettrone occupa di preferenza, un orbitale vuoto prima di appaiarsi con un altro elettrone.
L’ordine di occupazione degli orbitali è: 1s, 2s, 2p, 3s, 3p, 3d, 4s, 4p, 4d, 4f …
Esempi:
Idrogeno 1H: l'atomo di idrogeno ha un solo elettrone sul primo livello energetico. I numeri quantici sono:
n=1
l=0
ml=0
ms=+1/2
La notazione utilizzata per indicare un elettrone sul primo livello energetico e sull'orbitale s è: 1s1. La rappresentazione grafica:

Dove la freccia verso l'alto rappresenta un elettrone con spin +1/2 mentre la freccia verso il basso un elettrone con spin -1/2
Elio 2He: l'atomo di elio ha 2 elettroni sul primo livello energetico. I numeri quantici sono:
n=1
l=0
ml=0
ms=+1/2 e -1/2
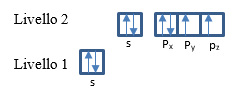
La notazione utilizzata per indicare 2 elettroni sul primo livello energetico e sull'orbitale s è 1s2. La rappresentazione grafica:
 Ossigeno 8O: l'atomo di ossigeno neutro ha 8 elettroni, 2 sul primo livello energetico e 6 sul secondo livello. I numeri quantici sono:
Ossigeno 8O: l'atomo di ossigeno neutro ha 8 elettroni, 2 sul primo livello energetico e 6 sul secondo livello. I numeri quantici sono:
n = 2
l = 0, 1
ml = -1, 0, +1
ms = +1/2 o -1/2
La notazione è 1s2 2s2 2p4, la rappresentazione grafica:
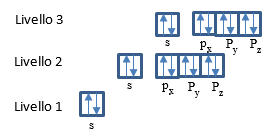
Argon 18Ar: l'argon neutro ha 18 elettroni, 2 sul primo livello energetico, 8 sul secondo livello e 8 sul terzo. I numeri quantici sono:
n = 3
l = 0, 1, 2
ml = -2, -1, 0, +1, +2
ms = +1/2 o -1/2
La notazione è 1s2 2s2 2p6 3s2 3p6, la rappresentazione grafica:
Notazione degli atomi utilizzata in chimica
Nella chimica si utilizzano le seguenti convenzioni:
- Numero di massa (A) = numero di protoni + numero di neutroni (nel calcolo della massa vengono trascurati gli elettroni relativamente molto più piccoli dei protoni e neutroni).
- Numero atomico (Z) = numero di protoni
Il numero di protoni e neutroni definisce:
- Atomi neutri: il numero di protoni è uguale al numero degli elettroni.
- Isotopi: il numero di neutroni è superiore a quello dei protoni.
La simbologia per descrivere gli atomi utilizzata in chimica è:
- apice a sinisra = numero di massa
- pedice a sinistra = numero atomico
- al centro = tipo di atomo
- apice a destra = carica dell'atomo
Normalmente un atomo ha lo stesso numero di protoni, neutroni ed elettroni, ma esistono delle eccezioni:
- Isotopi: il numero di protoni non è uguale a quello dei neutroni
- Anioni: il numero di elettroni è maggiore di quello dei protoni, quindi l'atomo ha carica negativa
- Cationi: il numero di protoni è superiore a quello degli elettroni, quindi l'atomo ha carica positiva
Se si parla di atomi e non di isotopi si può omettere il numero di massa (il numero di neutroni è uguale a quello dei protoni), nel caso dell'ossigeno ossigeno 8O
Se si parla di atomi neutri si può omettere la carica (apice a destra del simbolo dell’atomo), nel caso del carbonio 6C
Esempi:
OSSIGENO
168O0 trattandosi di atomo neutro 8O
O = tipo di atomo: Ossigeno
16 = numero di massa
8 = numero atomico (numero di protoni)
0 = carica dell'atomo, in questo caso nulla (numero di protoni = numero di elettroni)
ANIONE OSSIGENO
168O2- trattandosi di atomo carico 8O2-
O = tipo di atomo: Ossigeno
16 = numero di massa
8 = numero atomico (numero di protoni)
2- = carica dell’atomo, in questo caso negativa (8 protoni - 10 elettroni = -2)
CARBONIO
126C0 trattandosi di atomo neutro 6C
C = Carbonio
12 = numero atomico
6 = numero atomico (numero di protoni)
0 = carica dell'atomo, in questo caso nulla (numero di protoni = numero di elettroni)
ISOTOPO CARBONIO 13
136C0 trattandosi di isotopo neutro 136C
O = tipo di atomo: Ossigeno
13 = numero di massa
6 = numero atomico (numero di protoni)
0 = carica dell'atomo, in questo caso nulla (numero di protoni = numero di elettroni)
ISOTOPO CARBONIO 14
146C0 trattandosi di isotopo neutro 146C
O = tipo di atomo: Ossigeno
14 = numero di massa
6 = numero atomico (numero di protoni)
0 = carica dell'atomo,in questo caso nulla (numero di protoni = numero di elettroni)
| Tipo di atomo | Simbolo | Protoni | Neutroni | Elettroni |
| Ossigeno |
8O | 8 | 8 | 8 |
| Anione Ossigeno | 8O2- | 8 | 8 | 10 |
| Carbonio | 6C | 6 | 6 | 6 |
| Isotopo carbonio 13 | 136C | 6 | 7 | 6 |
| Isotopo carbonio 14 | 146C | 6 | 8 | 6 |
Una tavola periodica degli elementi si trova la seguente link: https://ptable.com/